주요우울장애(MDD) 환자에 대한 Brintellix® (vortioxetine)의 장기 유효성¹
주요우울삽화(MDE)로부터 회복된 환자 4명 중 1명은 1년 이내로 증상이 재발합니다.2 또한, 더 많은 수의 이전 삽화, 더 긴 MDE 지속 기간 및 더 중증의 우울 증상은 보통 향후 재발에 대한 예측 인자입니다.3
재발(relapse 및 recurrence)을 방지하기 위해서는 급성 치료에 반응을 보인 MDD 환자에 대해 급성 우울 삽화의 관해 후 최소 6개월의 장기 치료가 권장됩니다.3
5건의 long-term, open-label, flexible-dose extension 임상시험 데이터로 Brintellix® 단기(6~8주) 치료 후 MDD의 우울증 증상의 호전이 지속되는지 여부를 평가했습니다.1
아래 결과를 참조하십시오.
Brintellix®(5~20mg)는 장기간 MDD† 증상을 지속적으로 완화시킵니다.1,5
Change in MADRS total score for patients previously treated with Brintellix® 5-20 mg/day in controlled trials (acute) who continued treatment in open-label extension studies over 52 weeks1
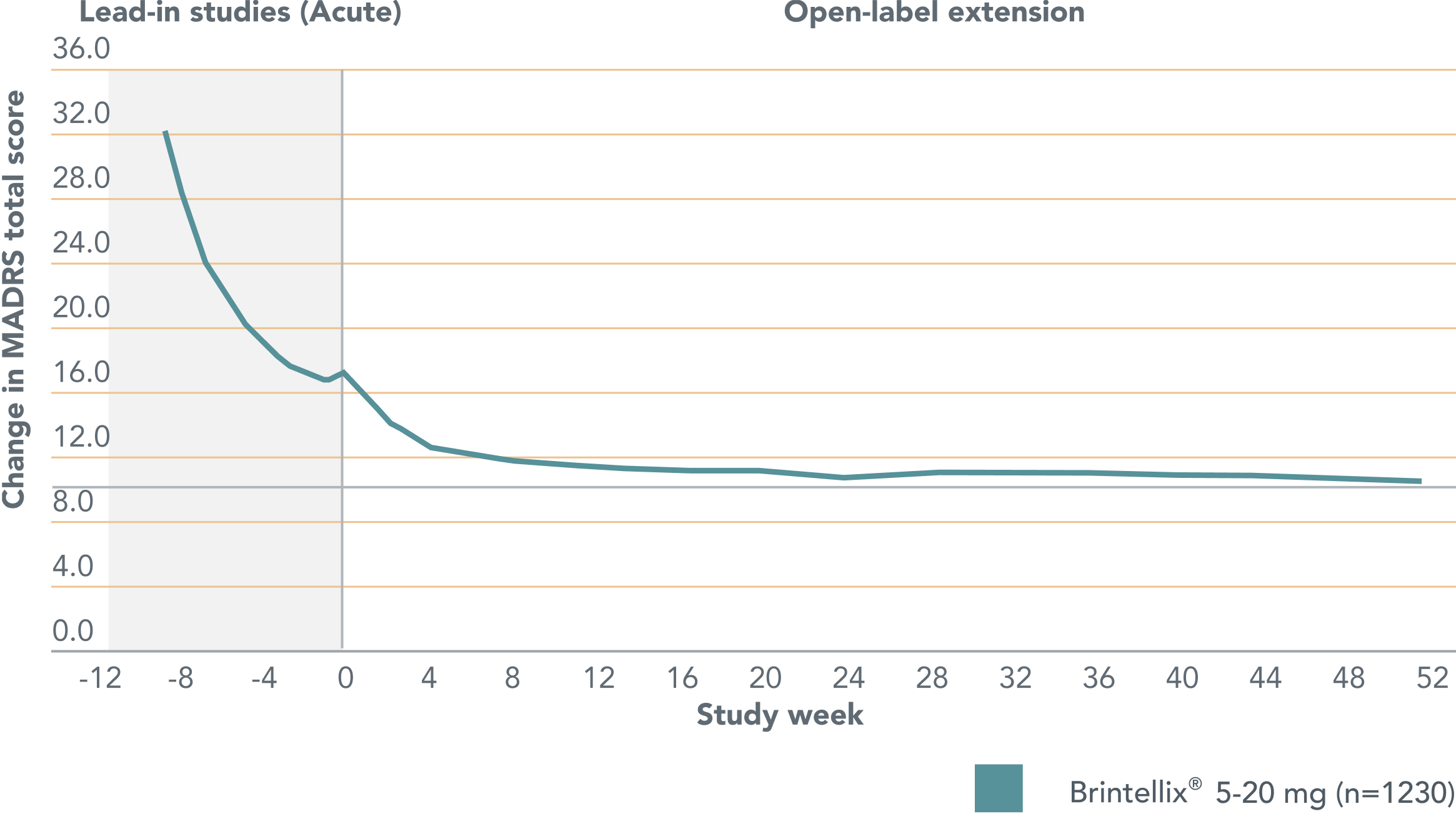
Adapted from Vieta E et al. 2017.
The horizontal dashed line indicates the cut point for remission (defined by MADRS total score <10). The vertical dashed line represents start of treatment in the extension study.
Brintellix® 단기(6~8주) 시험을 통해 확인된 MDD 증상 호전은 연장 시험 시작 지점부터 52주동안 지속적으로 유지되었습니다.
Adapted from Vieta E et al. 2017.
The horizontal dashed line indicates the cut point for remission (defined by MADRS total score <10). The vertical dashed line represents start of treatment in the extension study.
Brintellix® 단기(6~8주) 시험을 통해 확인된 MDD 증상 호전은 연장 시험 시작 지점부터 52주동안 지속적으로 유지되었습니다.

Brintellix®는 장기간 동안 일반적으로 내약성이 양호한 것으로 나타났으며1 이전 임상 시험과 일치하는 안전성 프로파일을 보였습니다.5,6 연장 시험 기간동안 가장 흔하게 보고된 투여후 발생 이상사례(TEAE)는 오심(16.6%)이었습니다. 발생률이 ≥5%인 다른 TEAE로는 두통(12.9%), 비인두염(9.4%), 설사(6.4%), 체중 증가(5.3%) 등이 있었습니다.1 연장 시험기간 중 TEAE로 인한 임상시험중단률은 낮았습니다(7.8%).1
Brintellix®는 장기간 동안 일반적으로 내약성이 양호한 것으로 나타났으며1 이전 임상 시험과 일치하는 안전성 프로파일을 보였습니다.5,6 연장 시험 기간동안 가장 흔하게 보고된 투여후 발생 이상사례(TEAE)는 오심(16.6%)이었습니다. 발생률이 ≥5%인 다른 TEAE로는 두통(12.9%), 비인두염(9.4%), 설사(6.4%), 체중 증가(5.3%) 등이 있었습니다.1 연장 시험기간 중 TEAE로 인한 임상시험중단률은 낮았습니다(7.8%).1

† MADRS로 측정.
‡ DESS 척도로 측정한) 중단 증상의 발생률과 TEAE로 인한 임상시험중단률에 기초함.5,6
Abbreviations:
MADRS, Montgomery-Åsberg depression rating scale; MDD, major depressive disorder; MDE, major depressive episode; TEAE, treatment-emergent adverse event.
† MADRS로 측정.
‡ DESS 척도로 측정한) 중단 증상의 발생률과 TEAE로 인한 임상시험중단률에 기초함.5,6
Abbreviations:
MADRS, Montgomery-Åsberg depression rating scale; MDD, major depressive disorder; MDE, major depressive episode; TEAE, treatment-emergent adverse event.

