At 36th ECNP Congress in Barcelona, we heard from two distinguished speakers in an industry symposium who spoke around the concept of moving ‘Beyond symptom relief in serious mental illness – personalizing approaches to functional recovery’. Both presentations had a particular focus on major depressive disorder. Professor Roger McIntyre (University of Toronto, Canada) spoke first to explain the need to recognize and address somatic comorbidities in serious mental illness.1 He was followed by Professor Narcís Cardoner (Universitat Autònoma de Barcelona, Spain) who discussed the need for physicians to help patients living with depression regain energy if they are to achieve functional recovery.2
바르셀로나에서 열린 제36회 ECNP 학술대회에서는 업계 심포지엄에서 '중증정신질환의 증상 완화를 넘어 - 기능 회복에 대한 맞춤형 접근법'이라는 개념을 중심으로 저명한 연사 두 명의 발표가 있었습니다. 두분 모두 주요우울장애를 중점적으로 다루었습니다. 먼저 로저 맥킨타이어 (Roger McIntyre) 교수(캐나다 토론토 대학교)는 중증정신질환에 동반되는 신체적 동반질환이 있음을 인식하고 이를 해결해야 할 필요성에 대해 설명했습니다.1 그리고 나르시스 카도너(Narcís Cardoner) 교수(스페인 바르셀로나 오토노마 대학)는 우울증 환자가 기능을 회복하려면 다시 에너지를 얻도록 의사의 도움이 필요하다고 제안했습니다.2
Recognizing and addressing somatic comorbidities with serious mental illness
중증정신질환에 동반되는 신체적 동반질환이 있음을 인식하고 해결하기
Serious mental illness (SMI), by definition, interferes with a person’s life and ability to function.3 It is therefore imperative that when helping a patient with an SMI regain functioning, we consider a specific therapeutic approach – one that is considered early; one that is personalized to the individual; and one that is holistic and considers factors that may impact recovery from an SMI.1
중증정신질환(SMI)은 개인의 삶과 기능을 방해하는 질환으로 정의됩니다.3 따라서 SMI 환자의 기능 회복을 도우려면 조기에 개입하고, 개인에게 맞춤화하며, 전인적이고, SMI 극복에 도움이 될 수 있는 구체적 치료법을 고려하는 것이 중요합니다.1
Major depressive disorder is a syndrome that rarely exists on its own
주요우울장애는 단독으로 존재하는 경우가 거의 없습니다.
In the first presentation, Professor Roger McIntyre explained that ‘major depressive disorder (MDD) is a syndrome that rarely exists on its own’, and that non-communicable diseases, such as heart disease, obesity, diabetes and anxiety, are commonly associated with SMI.4 Approximately 80 to 90% of people living with MDD will meet the criteria for another disorder in their lifetime.1 Data from over 30,000 individuals from a National Health Interview survey shows that in adults living with MDD, the odds ratio of having certain comorbid chronic medical disorders is high, including diabetes mellitus (DM, 1.96), coronary artery disease (CAD, 2.30) and chronic obstructive pulmonary disease (COPD, 3.21).4
첫 발표자인 로저 맥킨타이어 교수는 ‘주요우울장애(MDD)가 보통 다양한 증상을 보이는 질환’이며, 심장병, 비만, 당뇨병, 불안 등 비전염성 질환과 흔히 연관이 있다고 설명했습니다.4 그리고 MDD 환자의 약 80~90%는 일생 동안 다른 질환을 겪을 가능성이 높다고 합니다.1 미국 NHIS(National Health Interview Survey, 국민건강면접조사)를 통해 수집한 30,000명 이상의 데이터에 따르면, 성인 MDD 환자의 경우 당뇨병(DM, 1.96), 관상동맥질환(CAD, 2.30), 만성 폐쇄성 폐질환(COPD, 3.21) 등 일부 만성 동반질환을 겪을 확률이 높은 것으로 나타났습니다.4
These disorders are frequently referred to as comorbid conditions, a term Professor McIntyre questioned. ‘Given the fact we don’t know the pathology of major depressive disorder’, Professor McIntyre explained, ‘it is somewhat presumptive to use the phrase comorbidity.’ He then went on to explain that, when you come across a study that tells you a certain percentage of people have two or three other conditions, you begin to wonder if there is shared pathogenesis.
이는 흔히 동반질환 상태(comorbid conditions)라고 하는데, 맥킨타이어 교수는 이러한 용어 사용에 의문을 제기했습니다. 맥킨타이어 교수는 ‘주요우울장애의 병리를 확실히 알지 못한다는 점을 고려하면 동반질환(comorbidity)이라는 용어는 다소 추정적으로 사용한 것'이라고 설명했습니다. 그리고 특정 비율의 환자가 두세 가지 다른 질환을 갖고 있다고 보고한 연구가 있다며, 공통의 발병기전이 있는지 궁금증을 자아낸다고 말했습니다.
Professor McIntyre explained the concepts of homotypic and heterotypic continuity. Homotypic means the phenotype stays the same across time, as in Down’s Syndrome. Heterotypic means the phenotype changes how it presents across time. The speaker therefore questioned if in many cases, what we frequently refer to as comorbidity is in fact co-occurring syndromes that are better explained by heterotypic continuity.1
맥킨타이어 교수는 동형 및 이형 연속성이라는 개념에 대해 설명했습니다. 동형이란 다운증후군처럼 시간이 지나도 표현형이 동일한 것을 의미합니다. 이형이란 시간이 지나면서 표현형이 나타나는 방식이 변하는 것을 의미합니다. 따라서 맥킨타이어 교수는 대부분 흔히 동반질환이라고 부르는 것이 사실은 이형 연속성으로 더 잘 설명되는 동시발생 증후군(co-occurring syndrome)이 아닐지 의문을 제기했습니다.1
An example provided was obesity, which Professor McIntyre suggested ‘metastasizes to the brain’, with obesity and related conditions affecting depression more than in other populations.5 One link between obesity and depression is similar changes to resting state functional connectivity.5 Therefore, one area of research that Professor McIntyre’s research group is exploring is to what extent changes in the brain – at the cellular, structural, neural, and connectivity levels – link between conditions such as MDD and obesity.
맥킨타이어 교수는 비만을 예로 들며, 비만과 그 관련 질환들이 다른 사람보다 우울증을 앓는 사람에게 더 많은 영향을 미치고 이를 '뇌로 전이된다(metastasizes to the brain)'라고 표현했습니다.5 비만과 우울증 사이의 한 가지 연관성은 휴지기 기능 연결성(resting-state functional connectivity)과 비슷한 변화입니다.5 따라서 맥킨타이어 교수의 연구진이 탐구하고 있는 한 분야는 세포, 구조, 신경, 연결성 수준에서 뇌의 변화가 MDD와 비만과 같은 질환과 어느 정도 연관이 있는지 살펴보는 것입니다.
To what extent do changes in the brain – at the cellular, structural, neural, and connectivity levels – link between conditions such as MDD and obesity
세포, 구조, 신경, 연결성 수준에서 뇌의 변화가 MDD와 비만과 같은 질환과 어느 정도 연관이 있는 지 알아보는 것
Professor McIntyre then touched on the concept of loneliness. In recently published data from 2023, social isolation and loneliness has been shown to activate the inflammatory process making it a major risk factor for obesity, cardiovascular disease and SMI.6
그리고 맥킨타이어 교수는 외로움이란 개념에 대해서도 다루었습니다. 최근 발표된 2023년 데이터에 따르면, 사회적 고립과 외로움은 염증 과정을 활성화하여 비만, 심혈관 질환, SMI의 주된 위험 요인이 된다고 합니다.6
What is interesting about this study, highlighted Professor McIntyre, is that it provides a mechanistic link between depression and other diseases.6 For example, evidence from the UK Biobank suggests that inflammation via elevated C-reactive protein (CRP) levels may even have a causative role in the risk of depression.7 In another study, increased incidence of depression in patients with diabetes is linked to insulin resistance, which leads to increased levels of monoamine oxidases and dopamine function that may contribute to the risk of depression.8,9 This was perhaps unsurprising, suggested Professor McIntyre, when you consider there is a significant genetic overlap between endocrine-metabolic and depressive disorders.10
맥킨타이어 교수는 우울증과 다른 질환 사이의 기전적 관계를 제시한다는 점에서 이 연구가 흥미롭다고 강조했습니다.6 예를 들어, 영국 바이오뱅크의 자료에서는 C 반응성 단백질(CRP) 수치 상승을 통한 염증이 우울증 위험을 높이는 원인이 될 수도 있다고 합니다.7 또 다른 연구에 따르면, 당뇨병 환자의 우울증 발생률이 높은 것은 인슐린 저항성과 관련이 있다고 합니다. 모노아민 산화효소를 증가시키고 도파민 기능에 영향을 미쳐 우울증 위험을 높일 수 있다는 것입니다.8,9 맥킨타이어 교수는 내분비대사 질환과 우울증 간에 유의미한 유전적 중복(genetic overlap)이 있다는 점을 고려하면 이는 놀랍지 않은 일이라고 말합니다.10
All of this is important to consider, explained Professor McIntyre, because it shows the need to integrate our care when a patient presents with a serious mental illness. By targeting an SMI, such as depression, and its associated diseases, evidence suggests the outcomes are more favorable.11 It also allows us to consider how we design our treatments by targeting receptors that play a role in the development of many comorbid conditions.12
이는 환자가 SMI를 앓고 있으면 통합적인 진료가 필요하다는 의미이므로, 맥킨타이어 교수는 이 모두를 고려하는 것이 중요하다고 말합니다. 우울증을 비롯해 SMI와 그 관련 질환을 표적으로 하면 예후가 더 좋다고 합니다.11 또한 많은 동반질환 발병에 한 역할을 하는 수용체를 표적으로 삼아 치료제를 설계하는 방법도 고려할 수 있습니다.12
By targeting a SMI, such as depression, and its associated diseases, evidence suggests the outcomes are more favorable11
우울증을 비롯해 SMI와 그 관련 질환을 표적으로 하면 예후가 더 좋다고 알려져 있습니다.11
Regaining energy in depression to achieve functional recovery
우울증에서 기능 회복 달성을 위한 에너지 회복
In the second presentation, Professor Cardoner discussed lack of energy and fatigue in MDD, and how these are associated with poor functional recovery.2
두 번째 발표자인 카도너 교수는 MDD 환자의 에너지 부족과 피로에 대해 논하고 에너지 부족과 피로가 기능 회복의 어려움과 어떤 연관이 있는지 이야기했습니다.2
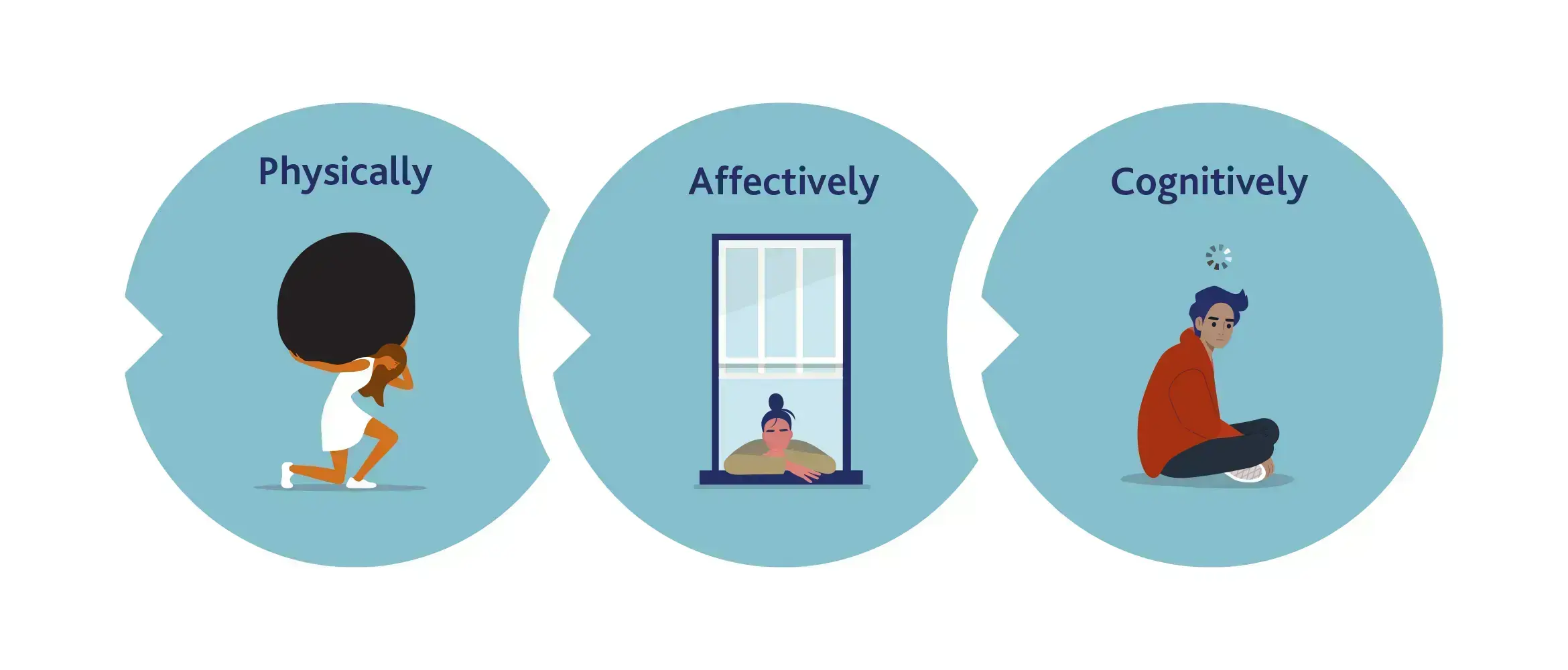
Defining fatigue is more difficult than we may expect, but the most common definitions include loss or lack of energy, feeling tired, physical feeling of lassitude, and exhaustion.13 In MDD, fatigue presents in different dimensions, such as physically (where it manifests as weakness and heaviness), affectively (where it manifests as decreased interest), and cognitively (where it manifests as slow thinking).14
피로를 정의하는 것은 생각보다 어렵지만, 가장 일반적인 정의로는 에너지 소실 또는 부족, 피로감, 신체적 무기력감, 탈진 등이 있습니다.13 MDD 환자에게 피로는 신체적(쇠약 및 무거움으로 발현), 정서적(흥미 감소로 발현), 인지적(느린 사고로 발현) 측면 등 여러 차원에서 나타납니다.14
There is debate about how prevalent fatigue is in depression. Some studies suggest it appears in approximately half of patients living with MDD, while others propose it to be as high as 95% of patients.15 For comparison, community-based studies suggest approximately 6 to 19% of the general population suffer from fatigue.16 Irrespective of its prevalence, evidence from one study in 2011 shows that fatigue is one of the most persistent symptoms in MDD.17
우울증 환자의 피로 유병률에 대해서는 의견이 엇갈립니다. 어떤 연구에서는 피로가 MDD 환자의 약 절반에서 나타난다고 주장하지만, 환자 95%까지 피로가 나타난다고 보고하는 연구도 있습니다.15 반면에 지역사회 기반 연구에서는 일반인 중 약 6~19%가 피로를 호소한다고 합니다.16 2011년의 한 연구에 따르면 그 유병률과 관계없이 피로는 MDD 환자에서 가장 지속적으로 나타나는 증상 중 하나라고 합니다.17
Fatigue is one of the most persistent symptoms in MDD17
피로는 MDD 환자에서 가장 지속적으로 나타나는 증상 중 하나입니다.17
In Professor Cardoner’s opinion, the etiology of a loss of energy in MDD is complex with links to neurotransmission, as well as the neuroendocrine, inflammatory and immune systems.2,18,19 The pathways causing fatigue in depression include disruptions in neuroinflammation and elevated cytokines, as well as impacts on the endocrine system, such as dysregulation in systems, including the hypothalamic-pituitary-adrenal (HPA) axis.18,19 However it is also important not to forget psychosocial factors, where stress, poor physical activity and diet, loneliness and absence of social support may all play a role.19
카도너 교수는 MDD 환자에서 에너지 소실이 나타나는 원인이 신경내분비, 염증, 면역 체계 뿐 아니라 신경 전달과도 관련이 있는 복합적인 것이라고 말했습니다.2,18,19 우울증 환자에서 피로를 유발하는 경로에는 신경 염증과 사이토카인 분비 증가와 같은 교란과 시상하부-뇌하수체-부신(HPA) 축을 포함한 각 계(system)의 조절 장애와 같은 내분비계에 대한 영향이 있습니다.18,19 그러나 스트레스, 부족한 신체 활동과 부실한 식단, 외로움, 사회적 지지의 부재 모두 중요한 심리사회적 인자임을 간과해서는 안 됩니다.19
Nonetheless, all of the symptoms of MDD are related to one of three neurotransmitters: serotonin, noradrenaline or dopamine.20 Loss of energy is associated with noradrenaline depletion, yet most treatments for MDD primarily target serotonin.20 So while relief from other symptoms is achieved with treatment, fatigue can linger and prevent the person from rejoining life’s activities.20 This is particularly important, suggested Professor Cardoner, given the challenges involved in the treatment of energy loss in depression involve the use of antidepressants that can elicit or worsen fatigue.21
그런데 MDD의 증상은 모두 세로토닌, 노르아드레날린 또는 도파민 등 3가지 신경전달물질 중 하나와 관련이 있습니다.20 에너지 소실은 노르아드레날린 고갈과 연관이 있지만, MDD 치료제 대부분은 일차적으로 세로토닌을 표적으로 합니다.20 따라서 MDD 치료제로 다른 증상은 완화시킬 수 있지만 피로는 지속되어 환자가 일상 활동을 힘들어할 수 있습니다.20 카도너 교수는 우울증 환자의 에너지 소실 치료 시 피로를 초래하거나 악화시킬 수 있는 항우울제를 사용하므로 이는 특히 중요하다고 말했습니다.21
Loss of energy is associated with noradrenaline depletion, yet most treatments for MDD primarily target serotonin20
에너지 소실은 노르아드레날린 고갈과 연관이 있지만, MDD 치료제 대부분은 일차적으로 세로토닌을 표적으로 합니다.20
Noradrenaline is implicated in cognition, motivation, and energy loss in depression.22 As such noradrenaline reuptake inhibition could play a specific role for those people living with depression suffering from a lack of energy.21
노르아드레날린은 우울증 환자의 인지, 동기 부여, 에너지 소실과 연관이 있습니다.22 따라서 노르아드레날린 재흡수를 억제하는 방식은 우울증 환자의 에너지 회복에 효과가 있을 수 있습니다.21
Professor Cardoner summarized his presentation by asking the audience to consider fatigue when treating depression, because pursuing a therapeutic approach that applies a focus on regaining energy, as well as addressing other symptoms, is important to restore functional recovery.
카도너 교수는 다른 증상의 해결 뿐 아니라 에너지 회복에도 중점을 둔 치료법을 찾는 것이 기능 회복에 있어 중요하기 때문에 참석자들에게 우울증 치료 시 피로를 고려할 것을 당부하며 발표를 마쳤습니다.
Educational financial support for this satellite symposium was provided by Viatris
Our correspondent’s highlights from the symposium are meant as a fair representation of the scientific content presented. The views and opinions expressed on this page do not necessarily reflect those of Lundbeck.